- La revista
- air jordan 5 island green releasing in november (2023) , SBD , air jordan 5 island green releasing in november
- Nike Nsw Therma - Fit Repel Puffer Jacket– JmksportShops - ladies length nike air max 95 essential black gold
- nike navy acg fw18 , nike navy acg fw18 Low Release Date - SBD
- where to buy air jordan shoes in dubai Low Reverse Liverpool DQ6400 , 300 Release Date - SBD - mens nike shox red and white color chart 6500
- Кроссовки nike air jordan 1 retro “travis scott” — цена 1399 грн в каталоге Кроссовки ✓ Купить женские вещи по доступной цене на Шафе , Украина #124847932 , NIKE AIR JORDAN FUTURE BLACK METALLIC GOLD-BLACK
- air jordan release dates
- Air Jordan 1 Heritage 555088 161 Release Date On Foot
- Travis Scott Fragment Air Jordan 1 Low DM7866 140 Release Date 4
- Gnarhunters Nike SB Dunk Low DH7756 010 Release Date On Foot
- adidas Ultra Boost 2022 COLD.RDY Magic Grey GZ0128 Release Date
- Presentación
- Políticas y proceso editorial
- Rigor científico y metodológico
- Producción y Administración
- Comités
- Normas presentación
- Consideraciones eticas
- Enviar artículo
- Hemeroteca
- Indexación
- Buscar
- Contacto
Farm Comunitarios. 2021 Jan 20;13(1):60-64. doi: 10.33620/FC.2173-9218.(2021/Vol13).001.07
Resumen de los avances de la vacuna frente a SARS-CoV-2
Introducción
Nos encontramos en plena carrera científica por el desarrollo de una vacuna segura y efectiva frente al nuevo virus SARS-CoV-2, y aunque ya hay laboratorios que van llegando a la meta, recibimos constantemente información a través de distintos canales, que, además, se actualiza a una gran velocidad, por lo que sería interesante elaborar un resumen o estado de situación que nos permita analizar con cierto criterio lo que está ocurriendo.
El desarrollo de una nueva vacuna requiere la integración de información acerca de diferentes aspectos: el ciclo biológico del patógeno, conocer su estructura, vía de entrada, interacción con los receptores celulares, sitios de replicación y los mecanismos de patogenicidad que den lugar a enfermedad; la epidemiología, que incluye la demografía de la infección, grupos de riesgo y ratios de enfermedad según edad, todo lo cual establece la población diana para la que se desarrolla la vacuna, y la respuesta inmunitaria del hospedador y los mecanismos de escape del patógeno, que determinan la selección del antígeno y la formulación de la vacuna.
Como se menciona anteriormente, para entender el mecanismo de acción de una vacuna, es fundamental conocer la estructura del virus al que nos enfrentamos, y las posibles vías de actuación que nos permitan desarrollar una vacuna efectiva. El SARS-CoV-2 es un RNA+ betacoronavirus, del subgénero sarbecovirus (1), con la siguiente estructura:
• Proteína N o nucleocápside: encargada de formar la nucleocápside, transducir señales al interior del virus, replicación de RNA y transcripción de mRNA.
• Proteína de membrana M y proteína de la envoltura E: juegan un papel importante ya que intervienen en el ensamblaje del virus.
• Proteína espicular S: es la responsable de la unión a la célula huésped. Es una glicoproteína espicular trimérica que se escinde en dos subunidades (S1 y S2) durante la infección. En el dominio S1 se encuentra la región de unión al receptor (RBD), mientras que S2 es responsable de la fusión de las membranas (1,2). Para entrar en la célula huésped, el virus se une mediante esta proteína a la proteína-enzima convertidora de angiotensina 2 (ACE2), que se expresa fundamentalmente en pulmones, corazón, riñones e intestino.
• ARN: el material genético consiste en una sola cadena de ácido nucleico ARN positivo.
• Envoltura: se trata de una envoltura de naturaleza lipídica, que puede ser disuelta por la acción de las moléculas de jabón.
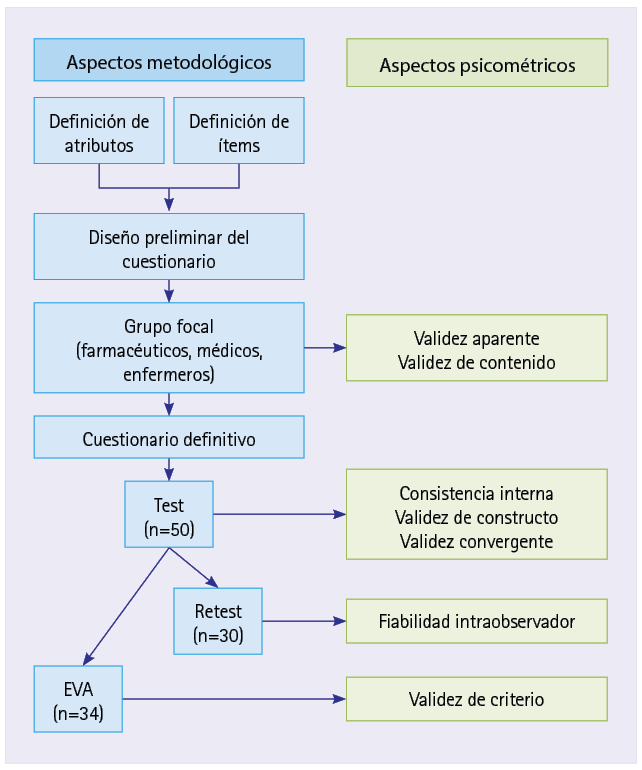
Figura 1 Estructura del virus SARS-CoV-2. (Cortesía de Bárbara Díaz Blanco)
El conocimiento de estas estructuras, junto a las imágenes obtenidas por microscopia crioelectrónica (premio Nobel de Química 2017) de la unión entre las proteínas S y ACE2 han permitido el desarrollo de distintas vacunas, así como el estudio de posibles antivirales (1,3,4).
Desarrollo de vacunas
Gracias a la experiencia previa en el desarrollo de vacunas, sabemos que para estimular la respuesta inmunitaria se puede utilizar el virus entero para desarrollar vacunas con el virus muerto o atenuado (5), o solamente partes antigénicas aisladas, que se describen a continuación, puesto que suponen la base para numerosos candidatos a vacunas debido a diversas ventajas, como su mayor seguridad y menor coste de producción:
Proteína S
Se sugiere que la proteína S o RBD es el antígeno más prometedor por encontrarse en la superficie, y además por poder ser reconocido directamente por el sistema inmune. La proteína entera (trimérica) frente a un solo monómero proporcionaría un mayor número de epítopos (porciones reconocidas por el sistema inmunitario) y, por tanto, le conferiría mayor inmunogenicidad (1,2,5). La inmunización RBD induce el bloqueo del reconocimiento con anticuerpos específicos, por ser la parte de la proteína que se une al ACE2 (5). No obstante, cualquiera de las partes de esta subunidad por separado es potencialmente útil en el desarrollo de una vacuna.
Epítopos de las células T y B de las proteínas S y N
Las porciones de las macromoléculas que son reconocidas por el sistema inmunitario, en concreto, las secuencias a las que se unen los anticuerpos, están altamente conservados entre SARS-CoV-2, responsable de COVID-19 y SARS-CoV, responsable del brote de 2003 de Síndrome respiratorio agudo grave (SARS). Es decir, los puntos de unión del sistema inmunitario a estos dos virus presentan similitudes estructurales. En este sentido, las vacunas diseñadas con estas secuencias, pueden ser eficaces contra SARS-CoV y SARS-CoV-2 por su alto grado de similitud genética y unión al mismo receptor ACE2 de la célula huésped (6). La protección cruzada con 2019-nCoV también puede desempeñar un papel protector en la evolución continua de la mutación del virus (1).
Proteína N o nucleocápside
Aunque es altamente antigénica, ya que el 89 % de los pacientes COVID+ han desarrollado anticuerpos, existen estudios contradictorios respecto a su capacidad antigénica, pero sin duda es un buen marcador diagnóstico (5).
Proteína M
Es capaz de neutralizar in vitro anticuerpos en pacientes con SARS, además el dominio transmembrana presenta un epítopo para las células T, capaz de inducir una respuesta inmune celular potente, por ello es un buen candidato para el estudio en la elaboración de una vacuna (5).
A pesar de que las propuestas actuales cubren casi todas las formas de investigación, y son numerosos los estudios que se están llevado a cabo en todo el mundo, no todas las partes antigénicas nombradas forman parte de las vacunas que se están desarrollando. Si nos centramos en los prototipos recogidos en el borrador de la Organización Mundial de la Salud (OMS), los tipos de vacunas en estudio son los siguientes:
Vacunas inactivadas o atenuadas
Gracias a la secuenciación del genoma del virus, permite la rápida generación de múltiples alternativas. Presentan numerosos componentes antigénicos y pueden inducir diversos estímulos inmunológicos frente al patógeno (5,7,8)
Vacunas de subunidades
Se obtienen mediante péptidos sintéticos o recombinantes. Incluyen a uno o más antígenos con fuerte capacidad inmunogénica o con una eficiente estimulación del sistema inmunitario del huésped. Son más seguras y fáciles de producir, pero habitualmente requieren de coadyuvantes para producir una respuesta inmune adecuada (5,7,8). Habitualmente están formadas por las subunidades mencionadas más arriba.
Vacunas de mRNA
Son una alternativa muy prometedora por su alta potencia, cortos ciclos de producción, bajo coste de manufactura y una administración segura. Se seleccionan los antígenos, se optimizan sus secuencias, secuenciación de nucleótidos modificados y se optimizan los sistemas de aplicación, como es el caso de la matriz de microagujas (9). El objetivo es usar este mRNA para expresar la Proteína S y el dominio RBD (5,7,8).
Vacunas de DNA
Se trata de plásmidos de DNA que codifican para uno o más antígenos. Son más complejos que los mRNA en su formulación, sin embargo, al tener que entrar en el núcleo, existe el riesgo de producción de mutaciones en el genoma del hospedador (7,8).
Vacunas de vectores vivos
Son virus vivos que expresan antígenos heterólogos, es decir, son moléculas homólogas presentes en especies no relacionadas filogenéticamente. Se caracterizan por la combinación de la potente inmunogenicidad de las vacunas atenuadas y la seguridad de las vacunas de subunidades. Se utilizan de forma amplia en la inducción de inmunidad in vivo (5,7,8).
Vacunas de péptidos sintéticos o epítopos
Estas vacunas contienen solamente ciertos fragmentos del antígeno intacto y son habitualmente fabricadas por síntesis química. Son fáciles de preparar y de realizar control de calidad; sin embargo, su bajo peso molecular y su complejidad estructural provocan una baja inmunogenicidad. Se requieren modificaciones estructurales, sistemas de administración, y coadyuvantes (5,7,8).
El desarrollo de una nueva vacuna es el resultado de un largo proceso que incluye diferentes etapas. Las fases iniciales suelen prolongarse entre uno y cinco años. Posteriormente siguen un desarrollo clínico y farmacéutico que puede durar entre 15 y 20 años hasta obtener la autorización para la comercialización (10). No obstante, desarrollar una vacuna con celeridad en plena pandemia requiere un cambio de paradigma, con un inicio rápido y muchos pasos ejecutados en paralelo antes de confirmar el éxito del resultado de otro paso (11). Además, según la OMS, las vacunas deben mostrar una reducción del riesgo de enfermedad de, al menos, el 50 %, con suficiente precisión para concluir que la verdadera vacuna tenga una eficacia superior al 30 %; esto significa que el intervalo de confianza del 95 % para el resultado del ensayo debe excluir una eficacia inferior al 30 %. Una vacuna que tiene un 50 % de eficacia podría reducir apreciablemente la incidencia de COVID-19 en los individuos vacunados, y podría proporcionar inmunidad de grupo. Por lo tanto, aunque una eficacia mucho mayor del 50 % sería mejor, la eficacia alrededor del 50 % representaría un progreso sustancial (12).
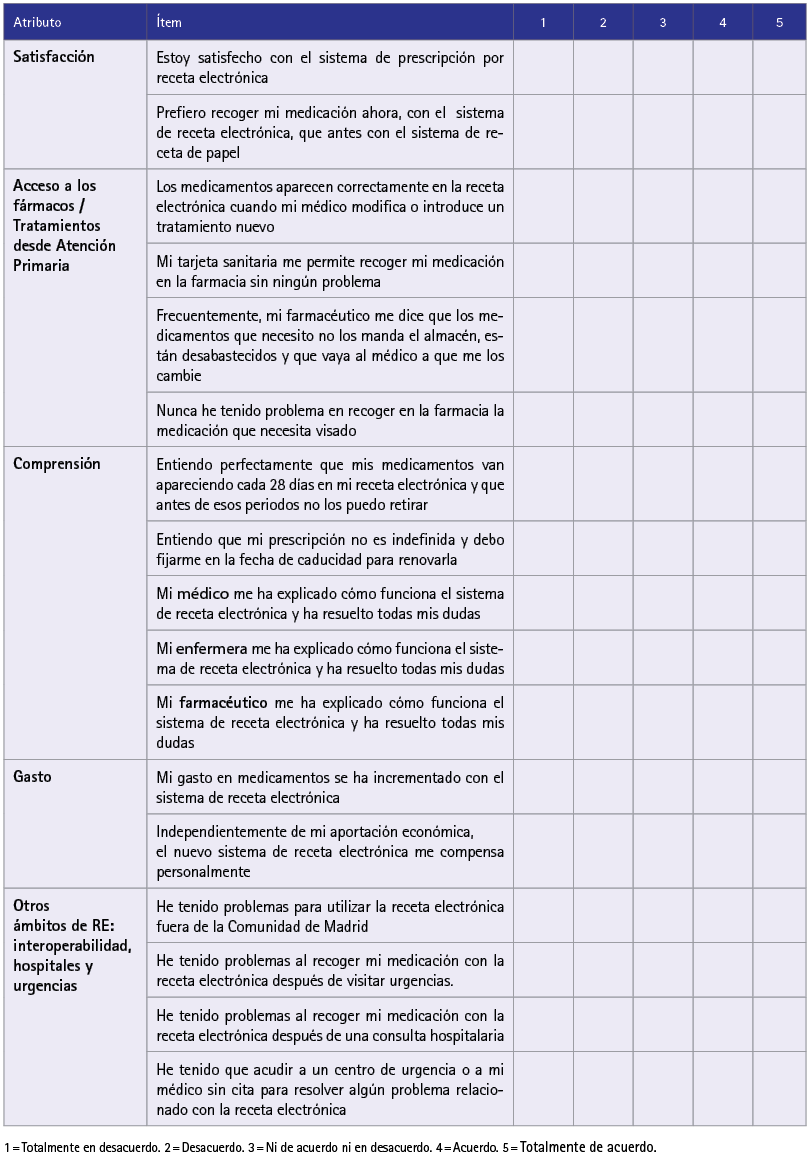
En el borrador proporcionado por la OMS, con finalidad informativa, a 8 de enero de 2021, constan 63 candidatos a vacuna frente a COVID-19 en evaluación clínica y 172 candidatos en evaluación preclínica, la OMS actualiza periódicamente esta información y se encuentra disponible en: https://www.who.int/publications/m/item/draft-landscape-of-COVID-19-candidate-vaccines. Según este borrador los tipos de candidatos a vacuna sometidos a ensayos clínicos son los que se indican en la tabla 1.
Tabla 1 Tipos de vacunas en investigación clínica a 8 de enero de 2021 según la OMS
Los principales retos de estas vacunas, además de la elección del antígeno, son minimizar los efectos indeseados de la inmunización y que se adecue a los individuos que son más susceptibles de contagio por SARS-CoV-2, como sanitarios o a aquellos individuos con mayor riesgo de desarrollar COVID-19 con peor pronóstico, tales como personas mayores de 60 años o pacientes con diabetes o hipertensión (6). Por ello elegir la forma adecuada, adyuvarla, los excipientes, la forma de dosificación, o la vía de administración puede suponer un impacto directo no solo en la respuesta inmune y la eficacia, sino también en la logística, manufactura, almacenaje y distribución (13). Un ejemplo de la necesidad de solucionar la parte logística es la estratégica colaboración entre ReiThera (Roma), LEUKOCARE (Múnich) y Univercells (Bruselas) que combinan su experiencia única en el desarrollo de vacunas basadas en vectores, formulación y fabricación de vacunas, para el desarrollo y producción de una vacuna a gran escala. Paralelamente a su desarrollo clínico, el consorcio comenzará a fabricar y almacenar la vacuna de forma coordinada para poder conseguir en el menor plazo de tiempo el mayor número de dosis de vacuna disponibles. Es por ello también que los candidatos a vacunas formadas por ácido nucleicos toman especial relevancia, ya que se pueden producir de forma rápida porque no requieren cultivo ni fermentación, sino que se utilizan procesos sintéticos (10), el reto más importante que presentan es su conservación pues necesitan temperaturas muy extremas.
De forma excepcional, debido a la emergencia sanitaria, los candidatos a vacunas están siendo sometidos al procedimiento de evaluación denominado rolling review o revisión continua, un mecanismo activado por la Agencia Europea del Medicamento (EMA) para acelerar los plazos de evaluación sin que suponga un perjuicio a las garantías de calidad, seguridad y eficacia establecidas en la legislación europea (14). De este modo la EMA evalúa los datos a medida que estén disponibles. A través de la revisión continua, se puede excepcionalmente comenzar evaluando los datos mientras el desarrollo está en curso. Cuando el desarrollo de la medicina está lo suficientemente avanzado para una solicitud de autorización de comercialización, el procedimiento de autorización puede tener lugar en un plazo muy corto marco de tiempo, porque los datos ya han sido examinados durante la revisión de la rueda de reconocimiento. Cada ciclo de revisión continua requiere alrededor de dos semanas, dependiendo de la cantidad de datos (15,16).
Vacunas comercializadas
Actualmente en Europa, gracias al procedimiento de evaluación mencionado, la EMA ha aprobado la comercialización condicionada de la vacuna contra la COVID-19 desarrollada por BioNTech en colaboración con Pfizer bajo el nombre comercial de Comirnaty®, para la prevención de COVID-19 en personas mayores de 16 años (17). Esta vacuna contiene una molécula de ARNm que codifica para la proteína S espicular presente en la superficie del virus del SARS-CoV-2 que el virus necesita para entrar en las células del cuerpo. Cuando una persona recibe la vacuna, algunas de sus células leerán las instrucciones del ARNm y producirán temporalmente la proteína espicular. El sistema inmunológico de la persona reconocerá entonces esta proteína como extraña y producirá anticuerpos y activará las células T (glóbulos blancos) para atacarlo. Si, más tarde, la persona entra en contacto con el virus del SARS-CoV-2, su sistema inmunológico lo reconocerá y estará listo para defender el cuerpo contra él, con una eficacia del 95 %. El ARNm de la vacuna no permanece en el cuerpo, sino que se descompone poco después de la vacunación (18).
Recientemente, también se ha aprobado la comercialización condicionada de la vacuna contra la COVID-19 desarrollada por Moderna en colaboración con el Instituto Nacional de Alergias y Enfermedades Infecciosas (EEUU), para la prevención de COVID-19 en personas mayores de 18 años (19). La vacuna ARNm-1273 de Moderna, conceptualmente es muy similar a la de Pfizer: se trata de una molécula de ARN mensajero que codifica la proteína S espicular, su lugar de anclaje a la membrana viral y el sitio de unión S1-S2. El ARNm está envuelto en una cápsula nanoprotéica de 4 lípidos que protege al ARNm de su degradación. Según los resultados obtenidos en los ensayos clínicos, el sistema inmunitario defenderá el organismo frente al virus SARS-CoV-2 con una eficacia del 94,1 % (20,21).
Como condición a la comercialización de ambas vacunas, los laboratorios deberán seguir aportando información acerca de los ensayos clínicos a lo largo de dos años, y además ampliar la información acerca del tiempo que permanece la protección, la prevención de casos graves, si previene infecciones asintomáticas, así como información en personas inmunodeprimidas, niños y embarazadas. Además, se están llevando a cabo estudios independientes que aseguren la seguridad y efectividad de las vacunas (17,19).
Cabe destacar que, a corto plazo, seguramente podamos disponer de una tercera vacuna comercializada en Europa, ya que la EMA ha recibido la solicitud de autorización condicional de comercialización de la vacuna COVID-19 desarrollada por AstraZeneca en colaboración con la Universidad de Oxford. De hecho, podría emitirse un dictamen sobre la autorización de comercialización antes del 29 de enero durante la reunión del Comité Científico de Medicamentos de Uso Humano de la EMA, siempre que los datos presentados sobre la calidad, la seguridad y la eficacia de la vacuna sean suficientemente sólidos y completos y que se presente con prontitud toda la información adicional necesaria para completar la evaluación (22).
Un horizonte prometedor se abre ante nosotros, con numerosas investigaciones tanto nacionales como internacionales. No obstante, reducir plazos, la producción masiva, y el almacenamiento controlado siguen suponiendo un reto. Sin embargo, la obtención de una vacuna no supone el control inmediato de la pandemia, sino más bien, un proceso gradual, puesto que se necesita un determinado porcentaje de población vacunada para frenar el contagio comunitario. Por eso, es de vital importancia cumplir las medidas higiénico-sanitarias de protección frente a la infección puestas en marcha y seguir siendo prudentes.
Referencias bibliográficas
1.Shi Y, Wang N, Zou QM. Progress and challenge of vaccine development against 2019 novel coronavirus (2019-nCoV). Zhonghua Yu Fang Yi Xue Za Zhi, 2020. 54(0): p. E029.
2.Dhama K, et al. COVID-19, an emerging coronavirus infection: advances and prospects in designing and developing vaccines, immunotherapeutics, and therapeutics. Human Vaccines & Immunotherapeutics, 2020: p. 1-7. doi:101080/21645515.2020.1735227
3.La ciencia de la Mula Francis [Sede web]. Francisco R. Villatoro; 7/3/2020 [accesoo 30/11/20] - La estructura 3D del receptor ACE2 que usa el coronavirus SARS-CoV-2 para infectar [Internet]. [1 página]. Disponible en: https://francis.naukas.com/2020/03/07/la-estructura-3d-del-receptor-ace2-que-usa-el-coronavirus-sars-cov-2-para-infectar/
4.University of Washington. Coronavirus spike proteins [vídeo en internet]. Youtube. 2017. [acceso 30/11/20]. Disponible en: https://www.youtube.com/watch?v=453zjjUllRg#action=share
5.Zhang J, et al. Progress and Prospects on Vaccine Development against SARS-CoV-2. Vaccines, 2020. 8(2): p. 153. doi:10.3390/vaccines8020153
6.Chen WH, et al. The SARS-CoV-2 Vaccine Pipeline: an Overview. Curr Trop Med Rep, 2020: p. 1-4. doi:101007/s40475-020-00201-6
7.Wang N, et al. Subunit Vaccines Against Emerging Pathogenic Human Coronaviruses. Front Microbiol, 2020. 11: p. 298. doi:103389/fmicb. 2020. 00298
8.Callaway E. The race for coronavirus vaccines: a graphical guide. Nature, 2020. 580(7805): p. 576. doi:101038/d41586-020-01221-y
9.Kim E, et al. Microneedle array delivered recombinant coronavirus vaccines: Immunogenicity and rapid translational development. EBioMedicine, 2020: p. 102743. doi:101016/j.ebiom.2020.102743
10.Urbiztondo L, Borràs E, Mirada G. Vacunas contra el coronavirus. Vacunas, 2020. 21(1): p. 69-72. Disponible en: https://www.sciencedirect.com/science/article/abs/pii/S157698872030008X?via%3Dihub
11.Centro de Investigaciones Biológicas Margarita Salas (CIB Margarita Salas) del Consejo Superior de Investigaciones Científicas (CSIC) [Online]. Madrid: CSIC-CIB; 24/5/2020 [acceso 30/11/20] Investigación. El Prof. Vicente Larraga lidera un proyecto para desarrollar una vacuna frente al SARS-CoV-2 basada en ADN recombinante [Internet]. [1 página]. Disponible en: https://www.cib.csic.es/es/news/investigacion/el-prof-vicente-larraga-lidera-un-proyecto-para-desarrollar-una-vacuna-frente-al
12.Krause P, et al. COVID-19 vaccine trials should seek worthwhile efficacy. The Lancet, 2020. 396(10253): p. 741-743. doi:101016/s0140-6736 (20)31821-3
13.Wang J, et al. The COVID-19 vaccine race: challenges and opportunities in vaccine formulation. AAPS PharmSciTech, 2020. 21(6): p. 1-12. https://dx.doi.org/10.1208%2Fs1 2249-020-01744-7
14.Agencia Española de Medicamentos y Productos Sanitarios [Online]. Madrid: MSCBS; 7/10/ 2020 [acceso 30/11/20] Acciones informativas. La EMA inicia la evaluación de la segunda propuesta de vacuna contra la COVID-19 [Internet]. [1 página]. Disponible en: https://www.aemps.gob.es/informa/notasinformativas/medicamentosusohumano-3/2020-medicamentosusohumano-3/la-ema-inicia-la-evaluacion-de-la-segunda-propuesta-de-vacuna-contra-la-covid-19/
15.European Medicines Agency [Online]. Amsterdam; EMA; [acceso 02/01/21] Fast-track procedures for treatments and vaccines for COVID-19 [Internet]. [1 página]. Disponible en: https://www.ema.europa.eu/en/documents/leaflet/infographic-fast-track-procedures-treatments-vaccines-covid-19_en.pdf
16.European Medicines Agency [Online]. Amsterdam; EMA; 1/10/2020 [acceso 30/11/20] News. EMA starts first rolling review of a COVID-19 vaccine in the EU [Internet]. [1 página]. Disponible en: https://www.ema.europa.eu/en/news/ema-starts-first-rolling-review-covid-19-vaccine-eu#:~:text=What%20is%20a%20rolling%20review
17.European Medicines Agency [Online]. Amsterdam; EMA; 21/12/2020 [acceso 02/01/21] EMA recommends first COVID-19 vaccine for authorisation in the EU [Internet]. [1 página]. Disponible en: https://www.ema.europa.eu/en/news/ema-recommends-first-covid-19-vaccine-authorisation-eu
18.European Medicines Agency [Online]. Amsterdam; EMA; 29/12/2020 [acceso 02/01/21] Comirnaty. COVID-19 mRNA vaccine (nucleoside-modified) [Internet]. [1 página]. Disponible en: https://www.ema.europa.eu/en/medicines/human/EPAR/comirnaty
19.European Medicines Agency [Online]. Amsterdam; EMA; 06/01/2021 [acceso 12/01/21] EMA recommends COVID-19 Vaccine Moderna for authorisation in the EU [Internet]. [1 página]. Disponible en: https://www.ema.europa.eu/en/news/ema-recommends-covid-19-vaccine-moderna-authorisation-eu
20.European Medicines Agency [Online]. Amsterdam; EMA; 06/01/2021 [acceso 12/01/21] COVID-19 Vaccine Moderna. COVID-19 mRNA Vaccine (nucleoside modified) [Internet]. [1 página]. Disponible en: https://www.ema.europa.eu/en/medicines/human/summaries-opinion/covid-19-vaccine-moderna
21.Sociedad Española de Quimioterapia: infección y vacunas [Online]. Madrid: Juan J. Picazo; 26/12/2020 [acceso 12/01/21] Vacunas frente al COVID-19 [Internet]. [12 páginas]. Disponible en: https://seq.es/wp-content/uploads/2020/12/vacunas-covid-2.5.pdf
22. European Medicines Agency [Online]. Amsterdam; EMA; 12/01/2021 [acceso 12/01/21] EMA receives application for conditional marketing authorisation of COVID-19 Vaccine AstraZeneca [Internet]. [1 página]. Disponible en: https://www.ema.europa.eu/en/news/ema-receives-application-conditional-marketing-authorisation-covid-19-vaccine-astrazeneca
Editado por: © SEFAC. Sociedad Española de Farmacia Clínica, Familiar y Comunitaria.
© Copyright SEFAC. Sociedad Española de Farmacia Clínica, Familiar y Comunitaria. Este artículo está disponible en la url https://www.farmaceuticoscomunitarios.org/ Este trabajo está bajo la licencia Creative Commons Attribution-NonCommercial-NoDerivatives 4.0 International License. Las imágenes u otro material de terceros en este artículo se incluyen en la licencia Creative Commons del artículo, a menos que se indique lo contrario en la línea de crédito. Si el material no está incluido en la licencia Creative Commons, los usuarios deberán obtener el permiso del titular de la licencia para reproducir el material. Para ver una copia de esta licencia, visite https://creativecommons.org/licenses/by-nc-nd/4.0/deed.es_ES


